Anglis yra vienas iš svarbiausių elementų mūsų planetoje, gyvybės pagrindas. Jos atomai sudaro įvairių organinių junginių pagrindą, kurie yra būtini visiems gyviems organizmams. Šiame straipsnyje aptarsime anglies savybes, alotropines atmainas, jos svarbą gyvybei ir pramonėje, taip pat anglies ciklą gamtoje ir jos junginių, ypač anglies dioksido, temperatūrines charakteristikas.
Anglies Alotropinės Atmainos
Anglis pasižymi įvairiomis alotropinėmis atmainomis, kurių kiekviena turi skirtingas fizikines ir chemines savybes. Yra žinomos trys natūraliosios anglies alotropinės atmainos:
- Grafitas: Pilkai juodos spalvos, neskaidrūs kristalai.
- Deimantas: Bespalviai skaidrūs kristalai, kiečiausia iš gamtoje esančių medžiagų. Deimantas yra izoliatorius: nepraleidžia elektros srovės ir šilumos.
- Amorfinė anglis: Tai amorfinė anglies forma, neturinti aiškios kristalinės struktūros.
Be natūralių atmainų, yra ir keletas sintetinių:
- Fulerenai: Molekulės, sudarytos iš anglies atomų, išsidėsčiusių sferinėmis arba elipsoidinėmis struktūromis.
- Anglies nanovamzdeliai: Cilindrinės struktūros, sudarytos iš susukto grafeno sluoksnio.
- Stikliškoji anglis: Amorfinė anglies forma, pasižyminti dideliu atsparumu karščiui ir cheminiams poveikiams.
- Karbinas: Linijinė anglies atmaina, sudaryta iš anglies atomų grandinės.

Anglies Kilmė ir Istorija
Su medžio anglimi žmogus susidūrė jau senovėje, tada, kai išmoko išgauti ugnį. Pavadinimas kilęs iš lotynų kalbos žodžio carbo - medžio anglys. Grafito pavadinimas kilęs iš graikų kalbos žodžio grapho - rašau. Žodis „deimantas“ kilęs iš graikų kalbos žodžio adamas - nenugalimas. Šis pavadinimas buvo pavartotas jau 16 m. m. e.
Anglies Svarba Gyvybei ir Jos Ciklas
Anglis yra gyvybės pagrindas mūsų planetoje. Tarp biogeninių elementų anglis užima ypatingą padėtį. Didžiąją kiekvieno organizmo kūno masės dalį (apie 98 %) sudaro ir į organinių junginių sudėtį įeina anglis, vandenilis, azotas, deguonis, fosforas, siera. Angliavandenius sudaro anglis, vandenilis ir deguonis, lipidus - anglis, vandenilis, deguonis, kai kuriuos fosforas ir azotas, baltymus - anglis, vandenilis, azotas, deguonis, siera, o nukleorūgštis ir ATP - anglis, vandenilis, azotas, deguonis ir fosforas. Per evoliuciją, Žemėje formuojantis gyvybei, anglies atomo savybės lėmė tai, kad anglis tapo pagrindine ląstelių biomolekulių sudedamąja dalimi. Įvairios struktūros anglies junginiai yra daugelio biomolekulių skeletas. Prie jo jungiasi įvairios funkcinės grupės (amino‑, karboksi‑, hidroksi‑, merkapto‑). Biopolimerų molekulių kai kurios dalys gali laisvai suktis apie viengubuosius ryšius tarp anglies atomų (C-C), todėl šios molekulės būna įvairios erdvinės struktūros. Tai lemia biomolekulių funkcijas. Augaluose anglis sudaro 42-45 % sausosios masės, gyvūnuose - 0,1-26 % gyvosios masės. Tos pačios rūšies organizmuose anglies kiekis priklauso nuo lyties, amžiaus, vystymosi stadijos. Be stabiliojo anglies izotopo 12C, augaluose kaupiasi ir radioaktyvusis izotopas 14C. Su maistu anglis patenka į gyvūnų ir žmogaus organizmą. Pavyzdžiui, 70 kilogramų sveriantis žmogus turi apie 12,6 kg anglies.
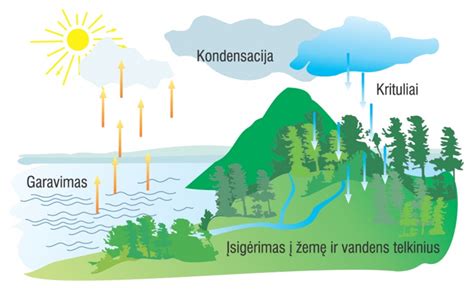
Anglies Ciklas. Anglies ciklas - tai nuolatinė anglies apytaka tarp gyvų organizmų ir juos supančios aplinkos. Augalai ir kai kurios bakterijos fotosintezės metu iš CO2 paima anglies atomus ir jie patenka į organinius junginius. Jais minta daugelis mikroorganizmų, grybai, gyvūnai. Visi gyvieji organizmai, oksiduodami organines maisto medžiagas (angliavandenius, baltymus, riebalus), CO2 pavidalu sugrąžina anglį į juos supančią aplinką. Iš žuvusių organizmų liekanų susidaro dirvožemio humusas, sapropelis, akmens anglys, nafta, gamtinės dujos. Deginant kurą anglis sugrąžinama į atmosferą. Suintensyvėjusi žmogaus ūkinė veikla (ypač 20 a. antroje pusėje), medžių kirtimas ir aplinkos teršimas sutrikdė anglies ciklą. Anglies dioksido kiekio didėjimas atmosferoje sukelia šiltnamio efektą.
Anglies Susidarymas ir Ištekliai
Anglims susidaryti reikia gausios augalijos ir drėgno bei šilto klimato. Tokios sąlygos susidarė karbono periode, kai Žemėje plačiai tyvuliavo vandenys, o jų pakrantėmis driekėsi pelkės, apaugusios paparčių, asiūklių, kitų priešistorinių medžių miškais. Augalai puvo, grimzdo į vandenį ir kaupėsi vandens telkinių dugne. Stovintis pelkių vanduo stokojo deguonies, todėl slopino bakterijų veiklą ir neleido augalams visai suirti. Tokioje aplinkoje susidarė durpės. Durpes klojo kitos sąnašos ir jas slėgė. Netekusi vandens ir dujų, veikiama aukštos temperatūros bei didelio slėgio, sudurpėjusi masė virto į anglis. Jei sąnašų storis yra 1 km, tai iš 20 m durpių sluoksnio susidaro 4 m storio rusvųjų anglių klodas. Jeigu augalinė medžiaga patenka į 3 km Žemės plutos gylį, tai toks pat durpių sluoksnis virs 2 metrų storio bituminių anglių klodu. Energijos ištekliai, kuriais šiandien naudojasi žmogus, kūrėsi milijonus metų. Anglis, nafta ir gamtinės dujos - visos iškastinio kuro rūšys - sukaupė Saulės energiją, pasiekusią Žemę galbūt prieš 500 milijonų metų. Jos susidarė iš augalinės kilmės medžiagos, kuri kito milijonus metų.
Anglis - pirmoji iškastinio kuro rūšis, kurios buvo daug kasama ir naudojama. Visa Vakarų visuomenės industrializacija buvo glaudžiai susijusi su anglių gavyba. Sužinoti, kiek iš tikrųjų po žeme esama anglių, beveik neįmanoma. Pasaulio anglių ištekliai vertinami trilijonais tonų. Tačiau šie skaičiai yra labiau teoriniai nei realūs. Apskaičiuota, kad žemėje glūdi veikiausiai 600 000 milijonų tonų tokių anglių, kurias galima iškasti šių laikų kasybos technika. Žinodami, kad XX a. 8-ojo dešimtmečio pradžioje pasaulinė anglių pramonė kasmet iškasdavo daugiau kaip 2000 mln. tonų antracito, o vien tik 1992 metais pasaulyje sudeginta 1065 tonų anglies. Apie 25 proc. šio kiekio buvo iškasama JAV; Europoje - mažiau. Šie skaičiai akivaizdžiai rodo, kad anglių pramonė gali ne tik gyvuoti, bet ir klestėti visą ateinantį šimtmetį. Moksliniais tyrimais apskaičiuota, jog išžvalgytus akmens anglies klodus, nepakitus vartojimo tempams, žmonija turėtu išeikvoti per 400 metų, tuo tarpu kitų neatsinaujinančio kuro rūšių resursai turėtų baigtis kur kas greičiau:
- Akmens anglys: Apytikslė resursų trukmė - 400 metų
- Nafta: Apytikslė resursų trukmė - 40 metų
- Gamtinės dujos: Apytikslė resursų trukmė - 60 metų

Šiuo metu anglys sudaro 28 proc. pasaulio energijos balanso. Anglys buvo pirmasis dideliais kiekiais naudotas iškastinis kuras. Jos lėmė pramoninę revoliuciją, kuri savo ruožtu turėjo įtakos anglių pramonės plėtotei - aprūpino ją tobulesne technologija, leido prasiskverbti iki gilesnių anglių klodų. Daugiau kaip 40 metų anglių naudojama vis mažiau. 1960 metais anglys teikė apie pusę pasaulio energijos; 1970 metais jų dalis jau buvo sumažėjusi 1/3 ir užleido vietą naftai ir gamtinėms dujoms, t.y. kitoms dviem svarbiausioms gaunamo kuro rūšims, vis daugiau tenkinančioms didėjančius energijos poreikius.
Akmens Anglies Savybės ir Panaudojimas Pramonėje
Akmens anglis, kaip ir nafta bei gamtinės dujos, yra organinė medžiaga. Nafta ir gamtinės dujos susidariusios daugiausia iš gyvūninės kilmės medžiagų (pavyzdžiui, planktono), o anglys susideda iš augalų liekanų, t.y. augalinės kilmės nuosėdinė uoliena; naudingoji iškasena. Akmens anglis susideda iš anglies (72-92%), vandenilio (2,5-5,7%), deguonies (1,5-15%), sieros (0,5-4%) ir azoto (~1,5%), taip pat truputį mineralinių priemaišų, kurios, anglims sudegus, sudaro pelenus. Anglyse esančias mineralinės medžiagas sudaro daugiausiai moliai, chloridai ir sulfidai. Pastarieji kelia itin didelį nerimą, nes, anglims degant, sudaro sieros dioksidą, kuris teršia atmosferą. Lakiosios medžiagos sudaro 2-45%. Drėgnis 4-14%. Peleningumas 2-45%. Tekstūra sluoksniuota, juostuota, tolygi. Spalva juoda, kartais su pilku plieninius arba tamsiai pilku atspalviu. Akmens anglys būna matinės arba stiklo, šilko blizgesio. Tankis 1280-1500 kg/m3. Degimo šiluma 30,5-36,8 MJ/kg. Pagrindinė akmens anglių technologinė savybė, apibūdinanti jų vertę, yra sukepamumas ir koksingumas.
Anglies perdirbimas. Akmens anglys perdirbamos terminiu ir cheminiu būdu. Terminis perdirbimas: sausąja distiliacija akmens anglys verčiamos lakiaisiais produktais ir koksu. Koksuojamos ne visos, o tik koksinės, riebiosios, suliesintos sukepančios ir dujinės akmens anglys. Akmens anglies koksavimas - vienas pagrindinių angliavandenilių gavimo būdų. Koksavimas vyksta kaitinant akmens anglį be oro apie 1000 °C. Koksavimui labiausiai tinka koksinė anglis. Lėtai kaitinant akmens anglį iki 250 °C išgaruoja H2O, išsiskiria CO ir CO2. Kaitinant iki 350 °C - į dujų pavidalą pereina deguto garai, o anglis tampa plastiška. Iki 550 °C vyksta plastiškosios anglies masės skilimas - skiriasi dujų produktai. Toliau kaitinant gauname koksą. Lakiosios medžiagos taip pat toliau skyla - vyksta polimerizacija ir kiti procesai. Jei perdirbame 1 toną akmens anglies, turėtume apytiksliai gauti 0,8 tonos kokso, iki 40 kg deguto, 10 kg benzeno, 3-4 kg NH4 ir 300 m3 koksavimo dujų. Koksas - kietos matinės juodos spalvos medžiaga. Be oro kaitinant akmens anglį išskiriamos lakiosios medžiagos, o kieta daug anglies turinti liekana vadinama koksu. Iš akmens anglių deguto frakcinės distiliacijos būdu gaunami benzino homologai, fenolis ir kitos medžiagos. Taip pat iš anglių gali būti gaminamas ir sintetinis benzinas bei kitų rūšių skystasis kuras. Akmens anglys verčiamos dujiniu kuru arba hidrinamos, t.y. perdirbamos į skystąjį kurą.
Kitas panaudojimas. Anglies junginiai yra svarbus energijos šaltinis; be to, ji yra įvairių chemijos pramonės produktų žaliava. Iš grafito daromi elektrodai, pieštukų šerdelės, juo dengiamos raketinių variklių detalės, išklojama chemijos pramonės aparatūra, lėtinami neutronai branduoliniuose reaktoriuose. Šlifuoti deimantai naudojami papuošalams, gręžimo įrankių antgaliams. Pastaruoju metu iš grafito pluošto ir polimerinių medžiagų gaminami kompozitai - labai tvirtos ir lengvos konstrukcinės medžiagos. Jų panaudojimo spektras labai platus - nuo teniso rakečių iki orlaivių. Grafito pluoštą galima pagaminti kaitinant aukštoje temperatūroje ir inertinių dujų atmosferoje kokį nors organinį pluoštą, pavyzdžiui, dirbtinį šilką. Toks gamybos procesas vadinamas grafitizacija. Metalurgijoje akmens anglys naudojamos dėl savo redukcinių savybių. Redukcijos procese dalyvauja ne tik anglis C, bet ir reaguojant susidarančios CO dujos. ZnO redukuojamas 1100 °C temperatūroje, t.y. aukštesnėje, nei cinko virimo temperatūroje. Ateinančiais dešimtmečiais akmens anglis turėtų išlikti Europos energijos šaltinių derinyje.
Anglies Gavyba ir Pasaulinė Rinka
Anglys kasamos 60 pasaulio šalių ir yra pasiskirsčiusios tolygiau nei nafta bei gamtinės dujos. Ilgą laiką akmens anglių daugiausiai išgaudavo JAV, Didžioji Britanija, Prancūzija, Vokietija, Lenkija ir kai kurios buvusios SSSR respublikos. Pastaraisiais dešimtmečiais akmens anglių pramonė daugelyje šių šalių išgyvena krizę. Didelės išlaidos ir konkurencija pasaulio rinkoje mažina anglių gavybą tradicinėse gavybos srityse: Rūro baseine (Vokietija), vidurio Anglijoje, šiaurės Prancūzijoje, Apalačiuose (JAV). Šiuo metu padidėjo Kinijos, Indijos, PAR ir Australijos anglių paklausa. Šiose šalyse daug akmens anglių kasama karjeruose (atviruoju būdu). Karjerus lengviau eksploatuoti, kasamų anglių savikaina mažesnė, todėl lengviau konkuruoti pasaulio rinkoje. Didžiausi akmens anglių baseinai: Huanghės (Kinija), Apalačų (JAV), Ruhro (Vokietija), Doneco (Ukraina), Aukštasis Silezijos (Lenkija), Minusinsko (Rusija), Pietų Velso (Didžioji Britanija). Anglis daugiausia naudoja jas kasančios šalys, o eksportuoja tos, kuriose anglių gavyba nereikalauja didelių išlaidų - Australija, JAV, PAR ir Kanada. Australijos ir PAR anglys Vakarų Europoje net tris kartus pigesnės nei vietinės. Dažnai didžiausius akmens anglių vartotojus (importuotojus) ir tiekėjus (eksportuotojus) skiria dideli atstumai, todėl per keletą dešimtmečių susiklostė akmens anglių transportavimo srautai. Pramoninė klasifikacija įvairiose šalyse yra skirtinga.
Temperatūros Sąvoka ir Anglies Junginių Virimo Temperatūros
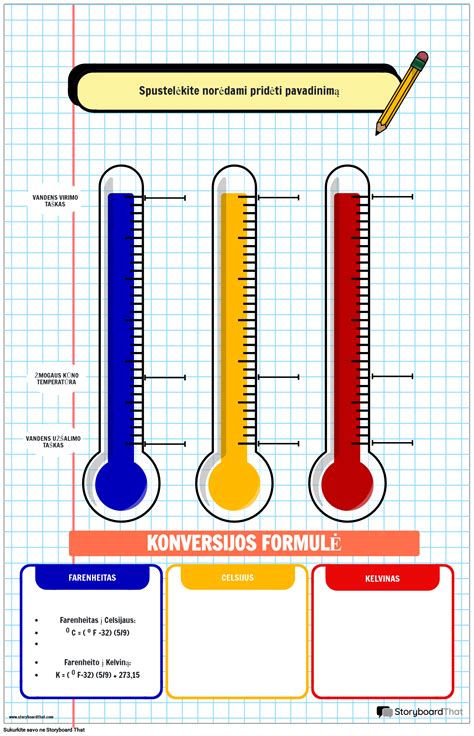
Trumpai tariant temperatūra tai objektą sudarančių atomų ir molekulių judėjimo greitis, kurio metu yra generuojama energija. Norint tinkamai paaiškinti šį reiškinį pirmiausiai reiktų turėti specifinių žinių fizikos mokslų srityje arba skirti nemažai laiko šių žinių paieškai. Labai tikėtina, kad didžioji dalis šio puslapio lankytojų puikiai suvokia ką reiškia temperatūra išreikšta celsijais. Būtent šį temperatūros matavimo vienetą mes dažniausiai naudojame kasdieniniame gyvenime. Daugelis net nesuabejodamas į klausimą "kokia yra vandens virimo temparatūra?" atsakytų "100°C”. Deja, prie skirtingo atmosferos slėgio šie matavimai kinta. Pavyzdžiui Everesto viršunėje vanduo pradės virti maždaug 68°C temperatūroje. Celsijaus matavimo vienetas yra plačiausiai ne mokslinėje aplinkoje naudojamas temperatūros matavimo vienetas, kuris yra žyminimas simboliu - °C. Yra priimta teigti, kad 0°C tai temperatūra kuomet užšala vanduo, o 100°C temperatūroje vanduo pradeda virti. Farengeito žymėjimo simbolis yra °F. Teigtina, kad matuojant farengeitais vanduo užšala 32°F temperatūroje, o užverda prie 212°F. Kelvinas (K) tai SI sistemos temperatūros matavimo vienetas. Žemiausia galima temperatūra kelvinais yra nulis laipsių dar žinoma kaip absoliutus nulis. Tai žemiausia įmanoma temperatūra, kurioje sustoja bet koks atomų ir molekulių judėjimas ir nutrūksta šiluminis spinduliavimas.
Anglies dioksidas (CO2) ir jo temperatūrinės savybės
Angliẽs dioksdas, angliẽs (IV) oksdas, angliẽs dvdeginis, angliãrūgštė, CO2, anglies ir deguonies junginys. Tai bespalvės, nedegios, silpnai rūgščios, sunkesnės už orą dujos. Jų lydymosi temperatūra yra -78 °C, o virimo temperatūra -57 °C. Normaliomis sąlygomis anglies dioksido tankis yra 1,98 kg/m3. Esant 20 °C temperatūrai ir 5,11 MPa slėgiui, CO2 virsta bespalviu, takiu skysčiu (tankis 1101 kg/m3), o atšaldytas iki -78,50 °C temperatūros - sniego pavidalo mase (sausuoju ledu; tankis 1560 kg/m3). Dujinis anglies dioksidas tirpsta vandenyje (1,45 g anglies dioksido 1 l H2O; susidaro anglies rūgštis H2CO3), daugelyje organinių tirpiklių, sieros, acto rūgštyse. Reaguoja su stipriomis bazėmis ir sudaro karbonatus. Leidžiant anglies dioksidą per įkaitintas anglis susidaro anglies monoksidas. 280 °C temperatūroje anglies dioksidas reaguoja su vandeniliu (katalizatorius CuO) ir sudaro metaną. Oro pertekliuje deginant anglį ir jos junginius, susidaro tik anglies dioksidas. Kita vertus, trūkstant deguonies (susidarius “riebiam mišiniui”), benzinas sudega nevisiškai, susidaro anglies monoksidas.
Laisvo CO2 yra ore (apie 0,03 % tūrio), mineralinių šaltinių vandenyje, vulkaninėse dujose, karbonatinėse uolienose - klintyje, kalcite, dolomite, marmure. Anglies dioksidas susidaro oksiduojantis organinėms medžiagoms (pūvant augalų ir gyvūnų liekanoms), deginant kurą, dalyvauja gamtoje vykstančioje anglies apytakoje. Į aplinką išskiriamą anglies dioksidą fotosintezei paima augalai. Anglies dioksidas gaunamas kalcio karbonatui reaguojant su druskos rūgštimi, deginant klintį (CaCO3 → CaO + CO2) arba vandens garais konvertuojant metaną (CH4 + 2H2O → CO2 + 4H2). Naudojamas sodos, karboksirūgščių, karbamido gamybai. Juo įsotinamas mineralinis, gydomųjų vonių vanduo, vaisvandeniai, yra gesinimo medžiagų sudedamoji dalis, lazerių darbo medžiaga. Sausasis ledas naudojamas kaip aušalas. Mažas kiekis žmogui nekenksmingas; įkvėpus daug galima apsinuodyti. Jei ore yra daugiau kaip 20 % anglies dioksido, apsinuodijus mirštama.
Anglies Izotopai ir Jų Panaudojimas
Gamtoje yra 2 stabilūs anglies izotopai. Kosminiai spinduliai dalį atmosferos azoto 14N paverčia anglies izotopu 14C; šio radioaktyvaus izotopo pusėjimo trukmė 5730 metų. Jis iki šiol plačiai naudojamas archeologinių radinių, medienos ir kitų medžiagų amžiui nustatyti. 14C kiekis augalų ir gyvūnų liekanose padeda nustatyti, kada jie gyveno. 14C naudojama fotosintezei, medžiagų kitimui ir apykaitai organizme tirti.
