Vanduo - gyvybės pagrindas Žemėje, pasižymintis unikaliomis savybėmis. Nors iš pirmo žvilgsnia vandens molekulė (H₂O) atrodo paprasta, jos unikalios savybės, įskaitant virimo temperatūrą, yra gyvybiškai svarbios gyvybės egzistavimui. Virimas yra fizikinis reiškinys, kurio metu skystis virsta dujomis (garais). Šis procesas vyksta, kai skysčio garų slėgis pasiekia aplinkos slėgį.
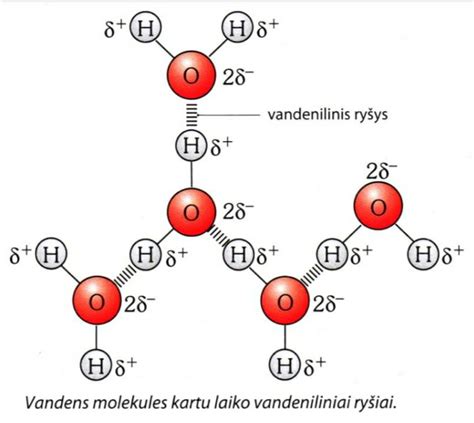
Vandens molekulės struktūra ir poliškumas
Vandens formulė yra H₂O, reiškinys, kad vieną vandens molekulę sudaro du vandenilio atomai ir vienas deguonies atomas. Vandenilio ir deguonies atomai vandens molekulėje yra susijungę kampu (104,5°), dėl skirtingo jų elektrinio neigiamumo molekulė yra polinė. Deguonies atomas yra labiau elektroneigiamas nei vandenilio atomai, todėl jis stipriau traukia elektronus, susidarančius kovalentiniam ryšiui. Dėl to prie deguonies atomo susidaro dalinis neigiamas krūvis (2δ-), o prie vandenilio atomų - dalinis teigiamas krūvis (δ+).
Vandenilinio ryšio susidarymas
Dėl polinės vandens molekulės sandaros, vandens molekulės traukia viena kitą. Vandenilinis ryšys susidaro tarp molekulių, kuriose yra vandenilio atomas, susijungęs su didelį elektroneigiamumą turinčiu atomu (pvz., deguonimi). Vandenyje vandenilinis ryšys susidaro tarp vienos molekulės deguonies atomo (turinčio dalinį neigiamą krūvį) ir kitos molekulės vandenilio atomo (turinčio dalinį teigiamą krūvį).
Kitas ir Keitė 😻 Augintinio rinkinys 45 serija | Filmukas vaikams lietuviškai
Vandenilinių ryšių įtaka virimo temperatūrai
Vandeniliniai ryšiai, nors ir silpnesni už kovalentinius ryšius, yra atsakingi už daugelį unikalių vandens savybių, įskaitant jo aukštą virimo temperatūrą. Norint paversti skystą vandenį dujiniu (garu), reikia įveikti šiuos vandenilinius ryšius tarp molekulių.
- Aukšta virimo temperatūra: Vandenilinis ryšys neleidžia molekulėms lengvai išsilaisvinti iš vandens paviršiaus. Tai sumažina garų slėgį. Vanduo nepradeda virti, kol garų slėgis nesusilygina su išoriniu slėgiu.
- Palyginimas su kitomis medžiagomis: Jei vandenilinių ryšių nebūtų, vanduo virtų esant -80°C, o užšaltų esant -100 °C temperatūrai, tad tokia gyvybė, kokia ji yra dabar, būtų neįmanoma. Standartinėmis sąlygomis (STP) vanduo būtų dujinėje būsenoje.
| Medžiaga | Molekulinė masė | Virimo temperatūra (°C) |
|---|---|---|
| Metanas (CH₄) | 16 | -161,5 |
| Vanduo (H₂O) | 18 | 100 |
Slėgio įtaka virimo temperatūrai
Virimo temperatūra priklauso nuo skysčio prigimties ir aplinkos slėgio. Uždaras puodas, pavyzdžiui, greitpuodis, neleidžia garams išeiti, todėl slėgis viduje didėja. Dėl didesnio slėgio vanduo užverda aukštesnėje temperatūroje (paprastai apie 112-120°C), o tai pagreitina virimo procesą.
Dėl puodo hermetiškumo, kaitinant vandenį susidarantys garai lemia, kad puodo viduje slėgis pakyla iki 1,6-2 atmosferų. Distiliavimas yra dar vienas procesas, kuriame vandeniliniai ryšiai tarp molekulių lemia skirtingų medžiagų virimo temperatūras, todėl šis metodas gali būti naudojamas medžiagoms atskirti.
