Virimas yra kasdienis reiškinys, kurį daugelis mūsų suvokia kaip savaime suprantamą dalyką. Tačiau pažvelgus giliau, virimas atsiskleidžia kaip sudėtingas fizinis ir cheminis procesas, apimantis energijos perdavimą, molekulių judėjimą ir fazių virsmus. Šis straipsnis skirtas išnagrinėti virimo procesą iš chemijos ir fizikos perspektyvų, siekiant suprasti, kas vyksta molekuliniame lygmenyje, kai skystis pasiekia savo virimo temperatūrą, taip pat aptarti bendruosius chemijos uždavinių sprendimo principus, kurie yra gyvybiškai svarbūs 11 klasės moksleiviams.
Chemija: mokslas apie medžiagas ir virsmus
Chemija yra fundamentali mokslo sritis, tirianti mus supančio pasaulio medžiagas, apimant jų savybes, sudėtį, struktūrą ir vykstančius virsmus, kurių metu keičiasi medžiagų sudėtis, o kartu ir energija. Ji aprėpia visą materijos įvairovę, pradedant subatominėmis dalelėmis ir baigiant sudėtingomis biologinėmis sistemomis. Pavyzdžiui, kvėpavimo procesas, kurio metu deguonis patenka į mūsų organizmą ir reaguoja su gliukoze, išskirdamas energiją, yra cheminis procesas. Arba metalų rūdijimas, kurio metu metalas reaguoja su ore esančiu deguonimi ir drėgme, sudarydamas oksidus - taip pat cheminis procesas.
Pagrindinės chemijos šakos
- Neorganinė chemija: Ši šaka koncentruojasi į neorganinių medžiagų, pavyzdžiui, mineralų, metalų ir jų junginių, tyrimą.
- Organinė chemija: Organinės chemijos objektas - anglies junginiai, kurie yra gyvybės pagrindas. Ši šaka yra itin svarbi, nes anglis gali sudaryti daugybę įvairiausių junginių, pasižyminčių skirtingomis savybėmis.
- Analizinė chemija: Tai chemijos šaka, tirianti medžiagų cheminę sudėtį. Analizinė chemija skirstoma į kokybinę analizę, kuri nustato, kokios medžiagos sudaro mėginį, ir kiekybinę analizę, kuri nustato, kiek kiekvienos medžiagos yra mėginyje.
- Fizikinė chemija: Ši šaka nagrinėja cheminių reiškinių fizikinius dėsningumus.
- Biochemija: Biochemija tiria cheminius procesus, vykstančius gyvuose organizmuose.

Chemijos ištakos siekia seniausias civilizacijas. Jau senovės egiptiečiai praktikavo įvairius cheminius procesus, gamindami stiklą, keramiką, dažus, kosmetiką ir vaistus. Viduramžiais alchemija buvo laikoma chemijos pirmtake. Tikroji mokslinė chemija pradėjo formuotis XVII-XVIII a., mokslo revoliucijos laikotarpiu. Periodinės elementų lentelės sukūrimas (1869 m., Dmitrijus Mendelejevas) leido ne tik sistemingai klasifikuoti tuo metu žinomus elementus, bet ir numatyti dar neatrastų elementų savybes, o tai vėliau buvo patvirtinta eksperimentiškai.
Chemijos mokymasis ir uždavinių sprendimas 11 klasėje
Mokantis chemijos skatinamas natūralaus smalsumo sužadinimas, mokymo(si) bei atradimo džiaugsmo patyrimas. Labai svarbi mokinių tiriamoji veikla, apimanti ne tik konkrečių užduočių atlikimą, bet ir tyrimų planavimą. Tai sudaro prielaidas mokiniams ugdytis kritinio ir kūrybinio mąstymo, problemų sprendimo gebėjimus, kelti asmeninius iššūkius, aiškinti(s) reiškinius, naudoti tyrimų metodus, daryti įrodymais grįstas išvadas ir kt.
Mokiniai skatinami atpažinti gamtamokslines problemas ir jas spręsti, vadovaujantis darnaus vystymosi, sveikos gyvensenos principais, atsakingai taikant įgytas chemijos ir kitų gamtos mokslų žinias ir gebėjimus įvairiose gyvenimo situacijose. Įgyvendinant Programą ugdomos šios kompetencijos: pažinimo, kūrybiškumo, komunikavimo, socialinė, emocinė ir sveikos gyvensenos, skaitmeninė, pilietiškumo, kultūrinė.
Plėtojamas gebėjimas taikyti tai, kas išmokta, mokiniams padedama suprasti įgytų žinių ir gebėjimų svarbą tolimesniam gyvenimui tiek pasirenkant profesiją, tiek būnant aktyviu piliečiu. Mokantis chemijos plėtojamas socialinis atsakingumas, puoselėjama meilė gamtai, mokoma būti išteklius tausojančiu vartotoju. Mokiniai mokomi nagrinėti ir vertinti gamtos apsaugą reglamentuojančius dokumentus ir skatinami sieti gamtamokslines veiklas su aktualiomis šalies ir pasaulio problemomis.
Chemijos svarba gyvenime, kasdienis naudojimas (chemija)
Virimas: fizikinis ir cheminis reiškinys
Virimas yra fizikinis reiškinys, kurio metu skystis virsta dujomis (garais). Šis procesas vyksta, kai skysčio garų slėgis pasiekia aplinkos slėgį. Virimo temperatūra priklauso nuo skysčio prigimties ir aplinkos slėgio. Normaliomis sąlygomis (101,3 kPa slėgyje) vandens virimo temperatūra yra 100 °C.
Įvairiems vienodos masės virimo temperatūros skysčiams paversti garais reikia skirtingo šilumos kiekio. Šilumos kiekis, kurio reikia 1 kg virimo temperatūros skysčio paversti garais, vadinamas savitąja garavimo šiluma. Savitoji garavimo šiluma žymima raide L, o jos matavimo vienetas yra J/kg.
Formulė virimo uždaviniams su šiluma:
Q = Lm, kur:
- Q - šilumos kiekis
- L - savitoji garavimo šiluma
- m - masė
Virimo metu skystyje susidaro burbuliukai. Skystyje yra ištirpusių dujų, kurios mažais burbuliukais nusėda ant indo dugno ir šylant vandeniui jos plečiasi, kyla į viršu ir sprogsta.
Kai kurių medžiagų virimo temperatūra
Virimo temperatūra yra esminė charakteristika, leidžianti nustatyti medžiagos fazės virsmus. Štai pavyzdžiai:
| Medžiaga | Virimo temperatūra (esant normaliam slėgiui) |
|---|---|
| Vanduo | 100 °C |
| Auksas | 2856 °C |
Uždavinių sprendimas chemijoje: formulės ir dėsniai
Sprendžiant chemijos uždavinius, svarbu žinoti pagrindines formules ir dėsnius. Štai keletas esminių, kurie yra aktualūs ir 11 klasės moksleiviams:
- Tirpinio masės dalis tirpale: w(medžiagos) = (m(medžiagos) / m(tirpalo)) * 100%
- Santykinis dujų tankis kitų dujų atžvilgiu: D = M1 / M2, kur M1 ir M2 yra dujų molinės masės.
- Dujų tūrių santykių dėsnis: Reaguojančių dujų tūrių santykis yra pastovus ir lygus mažų sveikų skaičių santykiui.
- Reakcijos lygtis: Pagal reakcijos lygtį galima apskaičiuoti reaguojančių arba susidarančių medžiagų kiekį, masę, tūrį, kai žinomas kurios nors reakcijoje dalyvaujančios medžiagos kiekis, masė, tūris.
Atomo sandara ir periodinis dėsnis
Norint suprasti cheminių procesų, įskaitant virimą, mechanizmus giliau, svarbu žinoti atomų sandarą ir periodinį dėsnį.
Atomas susideda iš branduolio ir elektronų. Branduolį sudaro protonai ir neutronai. Protonų skaičius atome yra lygus atominiam skaičiui. Elektronai išsidėstę aplink branduolį tam tikrais lygmenimis. Izotopai - tai to paties elemento atomų rūšys, turinčios vienodą protonų ir elektronų skaičių, bet skirtingą neutronų skaičių branduolyje.
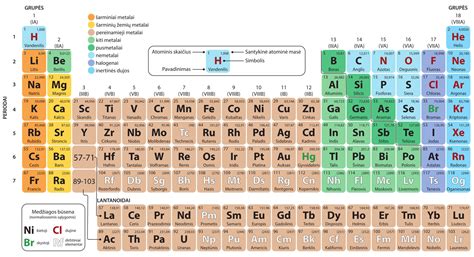
Periodinė elementų lentelė yra elementų klasifikavimo sistema, pagrįsta jų atominiu skaičiumi ir cheminėmis savybėmis. Vertikalūs stulpeliai lentelėje vadinami grupėmis, o horizontalios eilutės - periodais. Periodiškai kinta elementų savybės, tokios kaip metališkosios ir nemetališkosios savybės, atomų dydžiai, elementų junginių (oksidų ir nemetalų hidridų) bazinės ir rūgštinės savybės.
Cheminis ryšys
Cheminis ryšys yra jėga, laikanti atomus kartu molekulėse. Jo stiprumas ir tipas lemia medžiagų savybes. Pagrindiniai cheminių ryšių tipai:
- Elektrinis neigiamumas: Atomo gebėjimas pritraukti elektronus.
- Joninis ryšys: Ryšys tarp jonų, susidariusių, kai vienas atomas atiduoda elektroną kitam.
- Kovalentinis ryšys: Ryšys, susidarantis, kai atomai dalijasi elektronais.
- Vandenilinis ryšys: Silpnas ryšys tarp vandenilio atomo, prisijungusio prie elektroneigiamo atomo, ir kito elektroneigiamo atomo.
- Metališkasis ryšys: Ryšys tarp metalų atomų, kai elektronai laisvai juda tarp atomų.
Medžiagų klasės ir jų reakcijos
Chemijos uždaviniuose dažnai reikia atpažinti medžiagas, nustatyti jų savybes ir numatyti reakcijas. Svarbu gerai išmanyti neorganinius ir organinius junginius.
Neorganiniai junginiai
Neorganiniai junginiai skirstomi į keletą pagrindinių klasių:
- Oksidai: Junginiai, sudaryti iš elemento ir deguonies.
- Hidroksidai: Junginiai, sudaryti iš metalo ir hidroksilo grupės (OH-).
- Rūgštys: Junginiai, kuriuos tirpinant vandenyje susidaro vandenilio jonai (H+).
- Druskos: Junginiai, sudaryti iš metalo arba amonio katijonų ir rūgšties liekanos anijonų.
- Hidridai: Junginiai, sudaryti iš elemento ir vandenilio.
Rūgštys
Rūgščių tirpalų pH < 7. Rūgštys klasifikuojamos į deguonines ir nedeguonines. Joms būdingos šios reakcijos:
- Reakcijos su metalais: Praskiestos druskos ir sieros rūgštys reaguoja su metalais, išskirdamos vandenilį.
- Reakcijos su baziniais oksidais: Rūgštys reaguoja su baziniais oksidais, sudarydamos druskas ir vandenį.
- Reakcijos su šarmais: Rūgštys reaguoja su šarmais, sudarydamos druskas ir vandenį (neutralizacijos reakcija).
Rūgštis galima gauti iš rūgštinių oksidų dėl poveikio vandeniu arba iš atitinkamų druskų dėl poveikio koncentruota H2SO4.
Bazės
Bazių tirpalų pH > 7. Bazėms priskiriami junginiai, kuriuos tirpinant vandenyje susidaro OH- jonai. Jų reakcijos apima:
- Reakcijos su rūgštimis: Šarmai reaguoja su rūgštimis, sudarydami druskas ir vandenį (neutralizacijos reakcija).
- Reakcijos su rūgštiniais oksidais: Šarmai reaguoja su rūgštiniais oksidais, sudarydami druskas.
- Reakcijos su tirpiomis druskomis: Šarmai reaguoja su tirpiomis druskomis, kai susidaro netirpūs junginiai.
- Reakcijos su metalais: NaOH tirpalas reaguoja su metalais (Zn, Al), išskirdamas vandenilį.
Šarmus galima gauti iš metalų (Na ir Ca) reakcijų su vandeniu.
Oksidai
Oksidai klasifikuojami į bazinius, rūgštinius ir amfoterinius. Jų savybės ir reakcijos skiriasi:
- Baziniai oksidai: Reaguoja su rūgštimis, sudarydami druskas ir vandenį. Reaguoja su rūgštiniais oksidais, sudarydami druskas. Reaguoja su vandeniu, sudarydami hidroksidus.
- Rūgštiniai oksidai: Reaguoja su šarmais, sudarydami druskas ir vandenį. Reaguoja su baziniais oksidais, sudarydami druskas.

Dujos ir kiti elementai
Svarbu žinoti ir pagrindinių dujų bei elementų savybes bei reakcijas:
- Vandenilis (H2): Bespalvės, bekvapės dujos. Reaguoja su O2, Cl2, N2. Pramonėje gaunamas iš gamtinių dujų, vandens.
- Deguonis (O2): Bespalvės, bekvapės dujos. Alotropinės atmainos: Deguonis (O2), ozonas (O3). Reaguoja su H2, S, C, Ca, Cu. Gaunamas iš oro, vandens.
- Halogenai: Molekulės dviatomės (F2, Cl2, Br2, I2). Skiriasi spalva ir agregatinė būsena. Cl2 reaguoja su H2, metalais, vandeniu.
- Siera (S): Geltona kieta medžiaga. Reaguoja su O2, H2, metalais.
- Azotas (N2): Bespalvės, bekvapės dujos. Reaguoja su H2, O2.
- Anglis (C): Alotropinės atmainos: Deimantas, grafitas. Skiriasi sandara ir savybės.
Organiniai junginiai
Organinė chemija yra svarbi 11 klasės mokymo programos dalis, o užduotyse dažnai pasitaiko daug organinės chemijos užduočių, ypač nomenklatūros ir medžiagų atpažinimo.
- Angliavandeniliai: Junginiai, sudaryti tik iš anglies ir vandenilio.
- Sotieji angliavandeniliai (alkanai): Junginiai, turintys tik vienkartinius ryšius tarp anglies atomų.
Praktiniai uždaviniai ir laboratoriniai darbai
Chemijos pamokose ir konkursuose ypatingas dėmesys skiriamas praktiniams įgūdžiams ir eksperimentams.
Cheminiai indai ir prietaisai
Cheminiuose eksperimentuose naudojami įvairūs indai ir prietaisai. Svarbu juos ne tik pavadinti, bet ir tinkamai naudoti. Štai keletas pavyzdžių:
- Mėgintuvėlis
- Cheminė stiklinė
- Matavimo cilindras
- Pipetė
- Kūginė kolba
- Plokščiadugnė kolba
- Apvaliadugnė kolba
- Viurco kolba
- Matavimo kolbos
- Piltuvėlis
- Šaldytuvas
- Dalijamasis piltuvas
- Garinimo lėkštelė
- Kamštis su dujų nuvedamuoju vamzdeliu
- Laboratorinis stovas
- Spiritinė lemputė

Jonų atpažinimas
Chemijoje svarbu mokėti atpažinti įvairius jonus. Praktiniai metodai leidžia nustatyti, ar tirpale yra tam tikrų jonų. Pavyzdžiui, galima atpažinti H+, Ag+, Ba2+, OH-, Cl-, Na+, I- jonus. Taip pat svarbu užrašyti jų atpažinimo reakcijų lygtis.
Dujų gavimas ir atpažinimas
Laboratorijoje galima gauti ir atpažinti įvairias dujas: O2, H2, CO2, NH3, Etenas. Svarbu ne tik gauti ir surinkti šias dujas, bet ir užrašyti atitinkamų reakcijų lygtis. Medžiagų atskyrimui ir gryninimui naudojami metodai, tokie kaip garinimas, filtravimas, distiliavimas ir kristalinimas.
Akademiko Jono Janickio chemijos konkursas
Balandžio 7 d. KTU Cheminės technologijos fakultetas, Lietuvos Respublikos švietimo ir mokslo ministerija ir Lietuvos chemikų draugija organizuoja akademiko Jono Janickio chemijos konkursą. Konkurso tikslas - sudominti moksleivius chemijos mokslu, sudaryti jiems galimybes įvertinti savo žinias, susipažinti su KTU Cheminės technologijos fakultetu. Dalyvauti gali 10-12 klasių mokiniai. 9 klasių dalyvavimas kasmet svarstomas ir skelbiamas nuostatuose.
Tai vienos dienos chemijos konkursas. Po ryte atliktos teorinės dalies popiet atlikti eksperimentą kviečiamas tam tikras skaičius moksleivių (apie 100), kurie atrenkami pagal teorinės dalies įvertinimus. Nugalėtojai paskelbiami atsižvelgiant į teorijos ir eksperimento įvertinimus. Vakare teikiami apdovanojimai.
Užduotys dažniausiai lengvesnės nei olimpiadoje. Dažnai pasitaiko tirpalų uždavinių. 10-11 klasės gauna tas pačias, kuriose yra daug organinės chemijos užduočių (ypač nomenklatūros ir medžiagų atpažinimo). 12 klasės užduotyse daugiausia bendrosios chemijos. Eksperimento metu dažniausiai reikia atpažinti 3 neorganines medžiagas, pvz.: H2SO4, HNO3 ir NaCl. Dvyliktokams - titravimas. Moksleiviai, laimėję Janickio olimpiadoje, be konkurso įstoja į KTU chemijos fakultetą.
Konkursas vyks KTU Cheminės technologijos fakultete (Radvilėnų pl. 19), pradžia 10 val. Kaip patekti? Maždaug prieš mėnesį paprašyti chemijos mokytojo(-s) užregistruoti arba registruotis pačiam KTU.
Fizikos uždavinių ir dėsnių taikymas
Fizikoje tenka susipažinti ir išmokti taikyti daug formulių, tenka bandyti suvokti Archimedo jėgos, Niutono ar kitus dėsnius. Tenka atlikti nemažai laboratorinių darbų: kūnų tankio, varžos nustatymus ir pan. Kartais chemijos uždaviniams spręsti reikalingos ir fizikos žinios. Štai keletas pavyzdžių:
- Niutono Dėsniai: Uždavinys: 45kg masės krovinys juda horizontalia plokštuma, veikiamas 294N jėgos, kurios kryptis sudaro su horizontu 30laipsnių kampą. Krovinio trinties į plokštumą koeficientas 0,1. Koks judėjimo pagreitis?
- Elektrostatinė Sąveika: Uždavinys: Du taškiniai įelektrinti kūnai, kurių kiekvieno krūvis lygus 1 μC, nutolę 30 cm atstumu vienas nuo kito. Apskaičiuokite šių kūnų elektrostatinės sąveikos jėgą.
- Dujų Slėgis: Uždavinys: Kai slėgis buvo 760mmHg, po siurblio stūmokliu esantis oras užėmė 200cm³ tūrį.
tags: #uzdaviniai #is #virimo #11 #klase
