Virimas yra kasdienis reiškinys, kurį daugelis mūsų suvokia kaip savaime suprantamą dalyką. Tačiau pažvelgus giliau, virimas atsiskleidžia kaip sudėtingas fizinis ir cheminis procesas, apimantis energijos perdavimą, molekulių judėjimą ir fazių virsmus. Šis straipsnis skirtas išnagrinėti virimo procesą iš chemijos ir fizikos perspektyvų, siekiant suprasti, kas vyksta molekuliniame lygmenyje, kai skystis pasiekia savo virimo temperatūrą.
Chemija ir Medžiagos
Chemija - tai fundamentali mokslo sritis, tirianti mus supančio pasaulio medžiagas, apimant jų savybes, sudėtį, struktūrą ir vykstančius virsmus, kurių metu keičiasi medžiagų sudėtis, o kartu ir energija. Ji aprėpia visą materijos įvairovę, pradedant subatominėmis dalelėmis ir baigiant sudėtingomis biologinėmis sistemomis.
Chemijos ištakos siekia seniausias civilizacijas. Jau senovės egiptiečiai praktikavo įvairius cheminius procesus, gamindami stiklą, keramiką, dažus, kosmetiką ir vaistus. Tikroji mokslinė chemija pradėjo formuotis XVII-XVIII a., mokslo revoliucijos laikotarpiu.
Pagrindinės chemijos šakos yra:
- Neorganinė chemija: Ši šaka koncentruojasi į neorganinių medžiagų, pavyzdžiui, mineralų, metalų ir jų junginių, tyrimą.
- Organinė chemija: Organinės chemijos objektas - anglies junginiai, kurie yra gyvybės pagrindas. Ši šaka yra itin svarbi, nes anglis gali sudaryti daugybę įvairiausių junginių, pasižyminčių skirtingomis savybėmis.
- Analizinė chemija: Tai chemijos šaka, tirianti medžiagų cheminę sudėtį. Analizinė chemija skirstoma į kokybinę analizę, kuri nustato, kokios medžiagos sudaro mėginį, ir kiekybinę analizę, kuri nustato, kiek kiekvienos medžiagos yra mėginyje.
- Fizikinė chemija: Ši šaka nagrinėja cheminių reiškinių fizikinius dėsningumus.
- Biochemija: Biochemija tiria cheminius procesus, vykstančius gyvuose organizmuose. Ji nagrinėja biomolekulių, tokių kaip baltymai, angliavandeniai, lipidai ir nukleorūgštys, struktūrą, funkcijas ir sąveikas.
Atomų Sandara ir Periodinis Dėsnis
Norint suprasti virimo procesą giliau, svarbu žinoti atomų sandarą ir periodinį dėsnį.
Atomo Sandara
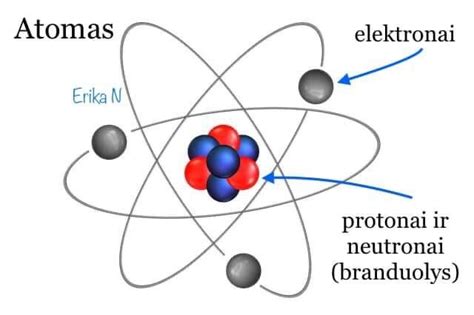
Atomas susideda iš branduolio ir elektronų. Branduolį sudaro protonai ir neutronai. Protonų skaičius atome yra lygus atominiam skaičiui.
Periodinis Dėsnis ir Periodinė Elementų Lentelė
Periodinė elementų lentelė yra elementų klasifikavimo sistema, pagrįsta jų atominiu skaičiumi ir cheminėmis savybėmis. Grupės: Vertikalūs stulpeliai periodinėje lentelėje. Periodai: Horizontalios eilutės periodinėje lentelėje.
Periodiškai kinta elementų savybės, tokios kaip:
- Metališkosios ir nemetališkosios savybės
- Atomų dydžiai
- Elementų junginių (oksidų ir nemetalų hidridų) bazinės ir rūgštinės savybės

Periodinės elementų lentelės sukūrimas (1869 m., Dmitrijus Mendelejevas) leido ne tik sistemingai klasifikuoti tuo metu žinomus elementus, bet ir numatyti dar neatrastų elementų savybes, o tai vėliau buvo patvirtinta eksperimentiškai.
Cheminis Ryšys
Cheminis ryšys yra jėga, laikanti atomus kartu molekulėse.
- Elektrinis neigiamumas: Atomo gebėjimas pritraukti elektronus.
- Joninis ryšys: Ryšys tarp jonų, susidariusių, kai vienas atomas atiduoda elektroną kitam. Joninė jungtis gali susidaryti tuo atveju, kai tarpusavyje jungiasi atomai, kurie turi labai skirtingą elektrinį neigiamumą. Joninė jungtis susidaro tarp atomų, kurių vienas linkęs elektronus atiduoti, o kitas-prisijungti. Lengvai atiduoda elektronus tų elementų atomai, kurių yra nedidelis jonizacijos potencialas.
- Kovalentinis ryšys: Ryšys, susidarantis, kai atomai dalijasi elektronais.
- Vandenilinis ryšys: Silpnas ryšys tarp vandenilio atomo, prisijungusio prie elektroneigiamo atomo, ir kito elektroneigiamo atomo.
Virimas: Fizikinis Reiškinys
Virimas yra fizikinis reiškinys, kurio metu skystis virsta dujomis (garais). Šis procesas vyksta, kai skysčio garų slėgis pasiekia aplinkos slėgį. Virimo temperatūra priklauso nuo skysčio prigimties ir aplinkos slėgio.

Virimo Temperatūra
Virimo temperatūra yra temperatūra, kurioje skystis pradeda virti. Normaliomis sąlygomis (101,3 kPa slėgyje) vandens virimo temperatūra yra 100 °C. Tačiau virimo temperatūra gali skirtis priklausomai nuo slėgio.
Virimo temperatūra priklauso nuo slėgio: kuo didesnis slėgis, tuo aukštesnė virimo temperatūra, ir atvirkščiai.
Skirtingų medžiagų virimo temperatūros skiriasi. Benzino virimo temperatūra normaliomis sąlygomis yra žemesnė nei vandens. Aukso virimo temperatūra yra labai aukšta.
Savitoji Garavimo Šiluma
Įvairiems vienodos masės virimo temperatūros skysčiams paversti garais reikia skirtingo šilumos kiekio. Šilumos kiekis, kurio reikia 1 kg virimo temperatūros skysčio paversti garais, vadinamas savitąja garavimo šiluma. Savitoji garavimo šiluma žymima raide L, o jos matavimo vienetas yra J/kg.
Formulė: Q = Lm, kur: Q - šilumos kiekis L - savitoji garavimo šiluma m - masė
Burbuliukų Susidarymas Virimo Metu
Virimo metu skystyje susidaro burbuliukai. Skystyje yra ištirpusių dujų kurios mažais burbuliukais nusėda ant indo dugno ir šylant vandeniui jie plečiasi, kyla į viršu ir sprogsta.

Virimo Temperatūros Priklausomybė Nuo Atominio Skaičiaus
Nors virimo temperatūra daugiausia priklauso nuo molekulinės masės ir tarpmolekulinių jėgų, atominis skaičius netiesiogiai daro įtaką šioms savybėms. Didėjant atominiam skaičiui, paprastai didėja ir atominė masė, o tai gali lemti stipresnes Londono dispersines jėgas tarp molekulių. Taip pat, didesnis atominis skaičius gali reikšti didesnį poliarizuojamumą, kas stiprina tarpmolekulines sąveikas.
Pavyzdžiui, aukso (atominis skaičius 79) virimo temperatūra yra labai aukšta (2856 °C). Tai susiję ne tik su dideliu atominiu skaičiumi, bet ir su reliatyvumo efektais, kurie veikia aukso elektronų orbitas ir stiprina atomų tarpusavio sąveiką.
Kita vertus, lengvesni elementai, turintys mažesnį atominį skaičių, paprastai turi žemesnę virimo temperatūrą. Pavyzdžiui, vandens (atominis skaičius deguoniui 8, vandeniliui 1) virimo temperatūra normaliomis sąlygomis yra 100 °C.
Reliatyvumo Įtaka Elementų Savybėms
Einšteino reliatyvumas kraipo erdvę, laiką, protus - ir periodinę lentelę. Prisiartinus prie aukso, kurio atominis skaičius yra 79, branduolio trauka yra jau tokia stipri, kad arčiausiai esantys elektronai zvimbia apie jį greičiu, prilygstančiu 80 % šviesos greičio. Tai padidina jų masę, tad jie sukasi arčiau branduolio ir uždengia tolesnius elektronus nuo jo traukos. Būtent iš čia atsirandantys poveikiai aukso sugeriamos šviesos bangų ilgiui lemia tai, kad auksas toks nepanašus į virš jo periodinėje lentelėje esančius brangiuosius metalus. „Tam, kad auksas skirtųsi nuo sidabro, reikia reliatyvumo,“ sako Pyykkö. Ir tai ne vienintelis atvejis, kai reliatyvumo efektai daro įtaką elementų savybėms. Šis pavyzdys iliustruoja, kaip atominis skaičius ir su juo susiję reiškiniai gali nulemti netikėtus elementų skirtumus.
Kai Kurių Medžiagų Virimo Temperatūros
Lentelė. Kai kurių medžiagų virimo temperatūros
| Medžiaga | Virimo temperatūra (°C) |
|---|---|
| Vanduo | 100 |
| Etanolis | 78.37 |
| Auksinis | 2856 |
Vandens Virimo Temperatūra: Praktiniai Aspektai
Vandens virimo temperatūra yra plačiai naudojamas orientyras. Daugelis mano, kad vanduo verda 100°C temperatūroje. Tačiau tai tiesa tik esant standartiniam atmosferos slėgiui.
Priklausomybė Nuo Slėgio
Vandens virimo temperatūra priklauso nuo slėgio. Tačiau jei kibirą vandens kelsime į kalno viršūnę, jis tikrai užvirs žemesnėje temperatūroje nei jūros lygyje. Norėdami nustatyti žemiausią vandens virimo temperatūrą, turime ieškoti vietos, kurioje yra rečiausias oras.
Mėnulio ir Planetų instituto duomenys rodo, kad aukščiausias taškas Žemėje yra Everesto kalno viršūnėje, 8849 metrų aukštyje. Tai vieta planetoje, kur vanduo užverda žemiausioje - tik 68 laipsnių Celsijaus - temperatūroje. Nors tai vis dar karštas vanduo, juo užplikyta kava būtų prasta, nes kavai reikia bent 87 laipsnių Celsijaus temperatūros.
Priklausomybė Nuo Priemaišų
Tyrėjai pažymi, kad vandenyje esančios priemaišos turi įtakos vandens molekulių tarpusavio sąveikai, galiausiai pakeičia viso tirpalo virimo tašką. Pavyzdžiui, įpylus druskos į vandenį, padidėja vandens virimo temperatūra, t. y., vanduo pradeda virti aukštesnėje nei 100°C temperatūroje. Tačiau druska nepadeda vandeniui greičiau užvirti - ji jį verčia virti lėčiau. Druska nepagerina vandens virimo greičio, tačiau ji svarbi dėl skonio.
Virimas Maisto Gamyboje
Vienas iš labiausiai paplitusių virimo pavyzdžių yra maisto gaminimas. Pavyzdžiui, verdant kiaušinį, svarbu žinoti, kiek laiko jį virti, kad jis būtų vidutiniškai išviręs.

Virimo Temperatūros Priklausomybė Nuo Slėgio: Clausius-Clapeyron Lygtis
Virimo temperatūra priklauso nuo aplinkos slėgio. Šią priklausomybę aprašo Clausius-Clapeyron lygtis:
dp/dT = ΔHvap / (TΔV)
čia: dp/dT - slėgio pokyčio priklausomybė nuo temperatūros; ΔHvap - garinimo entalpija (energija, reikalinga išgarinti vieną molį skysčio); T - absoliuti temperatūra (Kelvinais); ΔV - tūrio pokytis garinimo metu (garų tūris minus skysčio tūris).
Ši lygtis leidžia apskaičiuoti, kaip keičiasi virimo temperatūra, keičiantis slėgiui.
Supaprastinta Clausius-Clapeyron Lygtis
Jei darome prielaidą, kad garai yra idealiosios dujos ir skysčio tūris yra daug mažesnis už garų tūrį, Clausius-Clapeyron lygtis supaprastėja:
ln(p2/p1) = - (ΔHvap/R) * (1/T2 - 1/T1)
čia: p1 ir p2 - slėgiai; T1 ir T2 - atitinkamos virimo temperatūros (Kelvinais); ΔHvap - garinimo entalpija; R - idealiųjų dujų konstanta (8.314 J/(mol·K)).
Ši lygtis leidžia apskaičiuoti virimo temperatūrą esant kitokiam slėgiui, jei žinoma virimo temperatūra esant vienam slėgiui ir garinimo entalpija.
Virimo temperatūra, atmosferos slėgis ir garų slėgis
Skysčių Mišinių Virimo Temperatūra
Skysčių mišinių virimo temperatūra yra sudėtingesnė, nes ji priklauso nuo kiekvieno komponento garų slėgio ir koncentracijos mišinyje. Raoult'o dėsnis aprašo idealiųjų skysčių mišinių garų slėgį:
p_i = x_i * p_i^*
čia: p_i - komponento i garų slėgis virš mišinio; x_i - komponento i molinė frakcija mišinyje; p_i^* - gryno komponento i garų slėgis.
Mišinio virimo temperatūra yra ta, kurioje bendras garų slėgis virš mišinio yra lygus aplinkos slėgiui.
tags: #virimo #temperaturos #priklausomybe #nuo #atomo #skaiciaus
