Virimas - tai vienas iš svarbiausių fizikinių reiškinių, su kuriuo susiduriame kasdien, nuo maisto gaminimo iki sudėtingų pramoninių procesų. Tai procesas, kai skystis virsta dujomis (garais). Šiame straipsnyje detaliai panagrinėsime virimo esmę, jo temperatūrą, savitąją garavimo šilumą ir kitus svarbius aspektus, susijusius su šilumos perdavimu ir medžiagų savybėmis.
Kas yra virimas?
Virimas yra fazinis virsmas, kurio metu skystis pereina į dujinę būseną. Skirtingai nuo garavimo, kuris vyksta tik skysčio paviršiuje, virimas apima visą skysčio tūrį. Tai intensyvus procesas, kurio metu skysčio viduje susidaro ir kyla burbuliukai. Šie burbuliukai susidaro dėl skystyje ištirpusių dujų, kurios, šylant skysčiui, plečiasi, kyla į viršų ir sprogsta. Tai sukelia skysčio maišymąsi ir intensyvų garavimą.
Garavimas taip pat susijęs su vandens molekulių judėjimu. Vandens garai yra vandens molekulės, kurios įgavo pakankamai energijos, kad įveiktų skysčio paviršiaus įtempimą ir pereitų į dujinę fazę. Šis procesas vyksta nuolat, tačiau intensyvėja kylant temperatūrai.

Virimo temperatūra ir jos priklausomybė nuo slėgio
Virimo temperatūra - tai temperatūra, kurioje skystis pradeda virti. Ji priklauso nuo skysčio prigimties ir aplinkos slėgio. Normaliomis sąlygomis (1 atmosfera) vanduo užverda 100 °C temperatūroje. Tačiau virimo temperatūra gali kisti: kuo didesnis slėgis, tuo aukštesnė virimo temperatūra, ir atvirkščiai. Tai svarbu suprasti įvairiuose technologiniuose procesuose, kur slėgis gali skirtis nuo atmosferinio.
Skirtingų medžiagų virimo temperatūros skiriasi. Pavyzdžiui, aukso virimo temperatūra yra labai aukšta, o benzino virimo temperatūra normaliomis sąlygomis yra žemesnė nei vandens. Įvairiems vienodos masės skysčiams paversti garais reikia skirtingo šilumos kiekio, net jei jie verda skirtingose temperatūrose.
Savitoji garavimo šiluma
Vienas iš svarbiausių virimo proceso aspektų yra savitoji garavimo šiluma (L). Tai energijos kiekis, reikalingas vienam kilogramui skysčio paversti garais esant pastoviam slėgiui ir virimo temperatūrai. Ji parodo, kiek energijos reikia "įveikti" tarpmolekulinėms jėgoms skystoje fazėje ir pervesti medžiagą į dujinę būseną. Garavimo / kondensavimosi šiluma apskaičiuojama pagal formulę: Q = Lm, kur Q - šilumos kiekis (J), L - savitoji garavimo šiluma (J/kg), o m - skysčio masė (kg).
Didelė vandens savitoji garavimo šiluma (apie 2,26 MJ/kg prie 100 °C) reiškia, kad vandens garams susidaryti reikia daug energijos. Tai paaiškina, kodėl garų sukeltos nudegimai būna labai sunkūs - išsiskirianti latentinė garavimo šiluma yra didelė.
Savitoji šiluma
Nors šis straipsnis daugiausia dėmesio skiria virimo šilumai, svarbu suprasti ir bendresnę savitosios šilumos (c) sąvoką. Savitoji šiluma nurodo, kiek šilumos reikia, kad vieno medžiagos masės vienetas pakiltų vienu temperatūros laipsniu. Ji apskaičiuojama pagal santykį: c = q / (m · ΔT), kur q - perduotos šilumos kiekis, m - medžiagos masė, o ΔT - temperatūros pokytis. Dažniausi vienetai yra J/(kg·K).
Savitoji šiluma priklauso nuo temperatūros ir gali labai kisti arti fazių perėjimų (lydymosi, garavimo). Fazės pokyčio metu energija naudojama latentinei šilumai, o ne temperatūros kilimui.
Specifinės sąlygos: c_p ir c_v
Skiriamos dvi pagrindinės savitosios šilumos reikšmės: c_p - savitoji šiluma esant pastoviam slėgiui, ir c_v - savitoji šiluma esant pastoviam tūriui. Dujos pasižymi didesniu skirtumu tarp c_p ir c_v nei skysčiai ar kietosios medžiagos.
Matavimo būdai
Savitoji šiluma matuojama įvairiais metodais, įskaitant maišymo kalorimetriją, adiabatinį kalorimetrą ir diferencialinę skenuojančią kalorimetriją (DSC). Matavimų tikslumui svarbu kontroliuoti šilumos nuostolius ir užtikrinti tikslų temperatūros matavimą.
Pavyzdžiai ir tipinės reikšmės
- Vanduo (skystas, ~20 °C): apie 4184 J·kg⁻¹·K⁻¹
- Ledas (~0 °C): apie 2100 J·kg⁻¹·K⁻¹
- Aluminiumas: apie 900 J·kg⁻¹·K⁻¹
- Geležis: apie 450 J·kg⁻¹·K⁻¹
Šios vertės yra apytikslės ir gali skirtis priklausomai nuo temperatūros bei medžiagos grynumo.
Savitoji šiluma lemia veiksnius
Medžiagos savitąją šilumą keičia du veiksniai - slėgis ir temperatūra. Savitoji šiluma nustatoma esant standartiniam, pastoviam medžiagų slėgiui (paprastai atmosferos slėgiui) ir paprastai nurodoma esant 25 °C (298,15 K) temperatūrai. Savitoji šiluma yra intensyvioji savybė, nepriklausanti nuo medžiagos masės, kol temperatūra ir slėgis yra standartinėse nurodytose vertėse ir nevyksta fazių kaita.
Didelę įtaką savitosios šilumos dydžiui turi molekulinio lygmens energetiniai laisvės laipsniai. Kiekvienam laisvės laipsniui pasiekti reikalingas minimalus energijos kiekis. Skysčiai paprastai turi daugiau mažos energijos režimų ir daugiau energinių laisvės laipsnių nei kietosios medžiagos ir dauguma dujų, todėl jų savitosios šilumos dažnai būna didesnės.
Praktinė savitosios šilumos reikšmė
Savitoji šiluma yra svarbi inžinerijoje, klimato valdymėje, maisto pramonėje, medžiagų apdirbime ir energetikoje. Pvz., didelė vandens savitoji šiluma daro vandenį geru šilumos akumuliatoriumi. Medžiagų parinkimas šiluminiams izoliatoriams ar šilumos kaupikliais priklauso nuo jų savitosios šilumos.
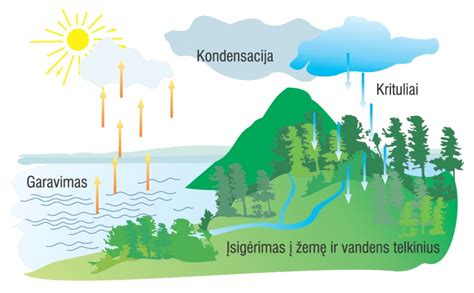
Garavimas gamtoje
Garavimas yra esminis procesas vandens apytakos rate. Šylantys ežerai, vandenynai, jūros ir kiti vandens telkiniai garuoja, taip pat garuoja vėstanti žemė. Per metus iš Žemės rutulio paviršiaus išgaruoja maždaug 500 000 km³ vandens. Šis procesas yra gyvybiškai svarbus klimato reguliavimui ir vandens ciklo palaikymui.
Rasa, rūkas ir debesys
Kai vandens garai ore atvėsta iki rasos taško, jie kondensuojasi, sudarydami smulkius vandens lašelius. Kai tai atsitinka ant žemės paviršiaus, susidaro rasa. Kai kondensacija vyksta ore, susidaro rūkas. Aukščiau atmosferoje, susikondensavę vandens garai sudaro debesis, kurie vėliau gali atnešti kritulius.
Evapotranspiracija
Evapotranspiracija - tai procesas, apimantis tiek garavimą nuo vandens telkinių ir dirvos paviršiaus, tiek transpiraciją - vandens garų išsiskyrimą iš augalų lapų. Tai svarbus vandens judėjimo gamtoje komponentas, ypač sausringuose regionuose.
Įdomūs faktai
- Mūsų kūno temperatūrą reguliuoja vandens garavimas iš organizmo, t.y. prakaitavimas; vanduo išgaruoja per odą, ir kūnas vėsta.
- Per metus iš Žemės rutulio paviršiaus išgaruoja maždaug 500 000 km³ vandens.
